Công Nghệ Sinh Học
Kỹ thuật mới mở ra tiềm năng cho thuốc tác động RNA
- Chi tiết bài viết
- Bài viết liên quan
Ngành công nghiệp dược phẩm hiện đang dành rất nhiều nguồn lực phát triển thuốc tác động lên protein. Con người có thể chữa bệnh gây ra do sự trục trặc của đại phân tử này bằng cách chèn một phân tử nhỏ vào vị trí hoạt động (active site) hay vào khe rãnh (pocket) có trên protein bị hư hỏng để can thiệp vào vào chức năng của phân tử này.
Nhưng tiếc rằng chỉ 15% protein có khe rãnh hoặc vị trí hoạt động phù hợp, trong khi 85% còn lại được xem như “không thể là mục tiêu cho thuốc”. Nhiều nhà nghiên cứu và các nhà phát triển thuốc đang nhận ra một giải pháp khác có lẽ là tác động lên protein liên quan đến bệnh nhưng ở cấp độ phân tử RNA thay vì cấp độ protein. (Xem thêm “Scientists Take Aim at Disease-Causing RNAs Using Small-Molecule Drugs,” The Scientist, 04/2019).
RNA thông tin (Messenger RNA) là một mục tiêu khả dĩ, vì chính chúng mã hóa cho protein và thậm chí trực tiếp can thiệp vào chu trình tế bào trong một vài căn bệnh. Nhưng những RNA khác cũng trong tầm ngắm của các nhà phát triển thuốc: các RNA không mã hóa, như những microRNA điều hòa biểu hiện gene, chúng cũng có thể là những phương án thay thế có giá trị. Sau tất cả, chỉ 1-2% bộ gen người được dịch mã thành protein, trong khi có tới khoảng 3/4 được phiên mã thành các RNA (PNAS, 104:19428–33, 2007).
“Với khả năng tác động lên RNA, bạn sẽ mở rộng đáng kể nguồn tiềm năng cho thuốc trúng đích” theo Rajeev Sivasankaran, trưởng ban khoa học thần kinh và khoa bệnh hiếm, thuộc viện Novartis Institutes for BioMedical Research ở Cambridge, Massachusetts.
Một phương án đang phát triển là sử dụng trình tự oligonucleotide đối mã (antisense oligonucleotides – viết tắt là ASOs), một chuỗi nucleic acid ngắn liên kết bổ sung đến RNA mục tiêu và khóa chúng lại hoặc thúc đẩy sự phân hủy. Nhưng phân tử cồng kềnh này không hề dễ dàng đi vào não và tủy sống, và chúng có thể còn gây giảm tiểu cầu, dẫn đến xuất huyết.
Các phân tử nhỏ ngược lại lại là những ứng viên thuốc tiềm năng hơn cho thử nghiệm. Thuốc phân tử nhỏ tác động lên RNA mặc dù không phổ biến nhưng không phải là không có: ví dụ, một số kháng sinh nào đó tác động lên RNA ribosome vi khuẩn. Một phân tử nhỏ bám vào vị trí có chức năng của một RNA có thể ngăn cản sự tương tác với ribosome hay những đối tác liên kết khác (other binding partners). Hay một phân tử nhỏ có thể thúc đẩy sự cắt và phân rã một mục tiêu RNA. Các nhà khoa học bây giờ đang áp dụng cả hai phương pháp sàng lọc thông lượng lớn (high-throughput screening approach) và phương pháp thiết kế hợp lý (rational design approach) để xác định phân tử nào sẽ có ảnh hưởng tới sinh học RNA. Dưới đây, The Scientist khảo sát vài kỹ thuật chính làm cho việc tác động đến RNA là bước lớn lao tiếp theo trong phát triển thuốc.
Cảm ứng cấu hình
Hiểu cấu trúc RNA có thể giúp các nhà khoa học tìm ra những khe rãnh (hốc) có trên chuỗi nucleic acid nơi mà thuốc có thể bám vào. Vài cấu trúc RNA có độ phức tạp tương tự như ở protein, Kevin Weeks nói – ông là nhà hóa học tại University of North Carolina ở Chapel Hill và là người đồng sáng lập Ribometrix, một công ty phát triển thuốc trúng đích RNA. Sự ghép cặp của các base nội phân tử tạo nên cấu trúc bấc hai, hình thành nên phân tử RNA có dạng xoắn kép và kẹp tóc. Chúng có thể tiếp tục hợp lại với nhau thành cấu trúc bậc ba phức tạp hơn như dạng đa xoắn (multihelix) hoặc giả nút (pseudoknot).
Weeks thiết kế một kỹ thuật dễ dàng sử dụng gọi là SHAPE (viết tắt của Selective 2′-Hydroxyl Acylation analyzed by Primer Extension) để thăm dò cấu trúc RNA (J Am Chem Soc, 127:4223–31, 2005; Nat Methods, 11:959–65, 2014). SHAPE giúp xác định phần nào của RNA lỏng lẻo và có thể tương tác với một thuốc thử, và chất nào có thể gắn lên cấu trúc khóa đi sự tương tác như vậy.
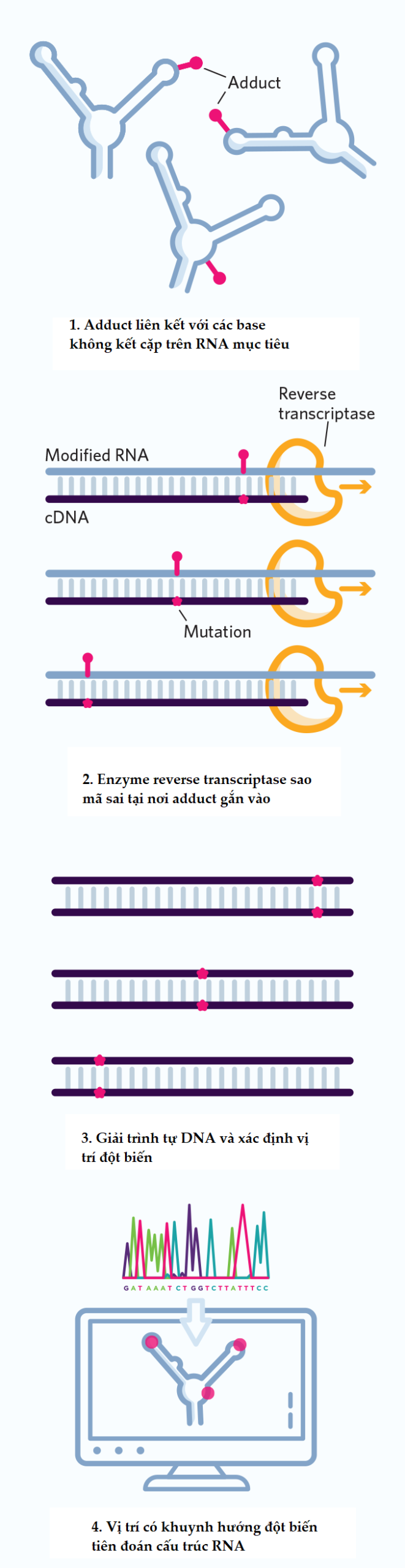
Thuốc thử, trong trường hợp này, là một chất trong bộ sưu tập các hóa chất tiềm năng có khả năng gắn với bất kỳ nucleotide nào trong bốn nucleotide A, U, G và C có trên RNA, gắn mỗi nucleotide với một chất gọi là 2’-O-adduct. Mẫu chốt ở đây là “Nó chỉ phản ứng với RNA tại những nucleotide linh động về cấu hình”. Ví dụ, trong một cấu trúc kẹp tóc RNA, các nucleotide kết cặp bổ sung dọc theo thân (dạng xoắn) sẽ được bảo vệ, còn các nucleotide ở đầu vòng loop thì tự do nên có thể can thiệp bằng thuốc thử.
Kết quả là một phân tử RNA trong đó có base bị đánh dấu với adduct, và những cái khác thì không. Sau đó, Weeks cùng nhóm dùng enzyme phiên mã ngược (reverse transcriptase) để tạo bản sao DNA từ phân tử RNA đó. Khi enzyme di chuyển dọc sợi RNA, nó sao mã sai tại nơi các base bị đánh dấu, đặt vào các nucleotide không phù hợp. Khi giải trình tự sợi DNA, các lỗi này hiện ra như là những đột biến, và chỉ ra vị trí nào trên sợi RNA ban đầu nơi có cấu hình linh động (Hình 1).
Các nhà nghiên cứu có thể nhập trình tự của họ vào phần mềm, truy cập miễn phí trên website của Week, để dự đoán cấu trúc. Theo Weeks, nó “khá là chính xác, nhưng không hoàn toàn 100%”. Kỹ thuật này tiến hành được cả trong ống nghiệm và bên trong tế bào.
Thẳng tới sàng lọc
Trong các đợt sàng lọc số lượng lớn gần đây, Novartis tình cờ phát hiện các phân tử nhỏ gắn với RNA và hệ thống cắt nối pre-mRNA (spiceosome) làm giảm nhẹ khiếm khuyết cắt nối (slicing defects) có liên quan đến chứng teo cơ cột sống (Nat Chem Biol, 11:511–17, 2015). Những nhà nghiên cứu này mặc dù không có chủ ý đi tìm những phân tử gắn lên RNA. Nhà sinh hóa Amanda Garner thuộc University of Michigan ở Ann Arbor ban đầu thiết kế là để sàng lọc các RNA. Đặc biệt cô sau đó lại chú ý đến những phân tử nhỏ liên kết với microRNA.
Phương pháp của cô là một dạng được biến đổi từ kỹ thuật ELISA (enzyme-linked immunosorbent assay), sử dụng kháng thể phát hiện peptide hoặc protein. Nó được gọi là catalytic enzyme-linked click-chemistry assay, hoặc cat-ELCCA (Chem Commun, 52:8267–70, 2016). Thử nghiệm này phát hiện các phân tử nhỏ có thể can thiệp vào sự trưởng thành của microRNA từ dạng pre-miRNA cấu hình kẹp tóc thành dạng microRNA mang chức năng.
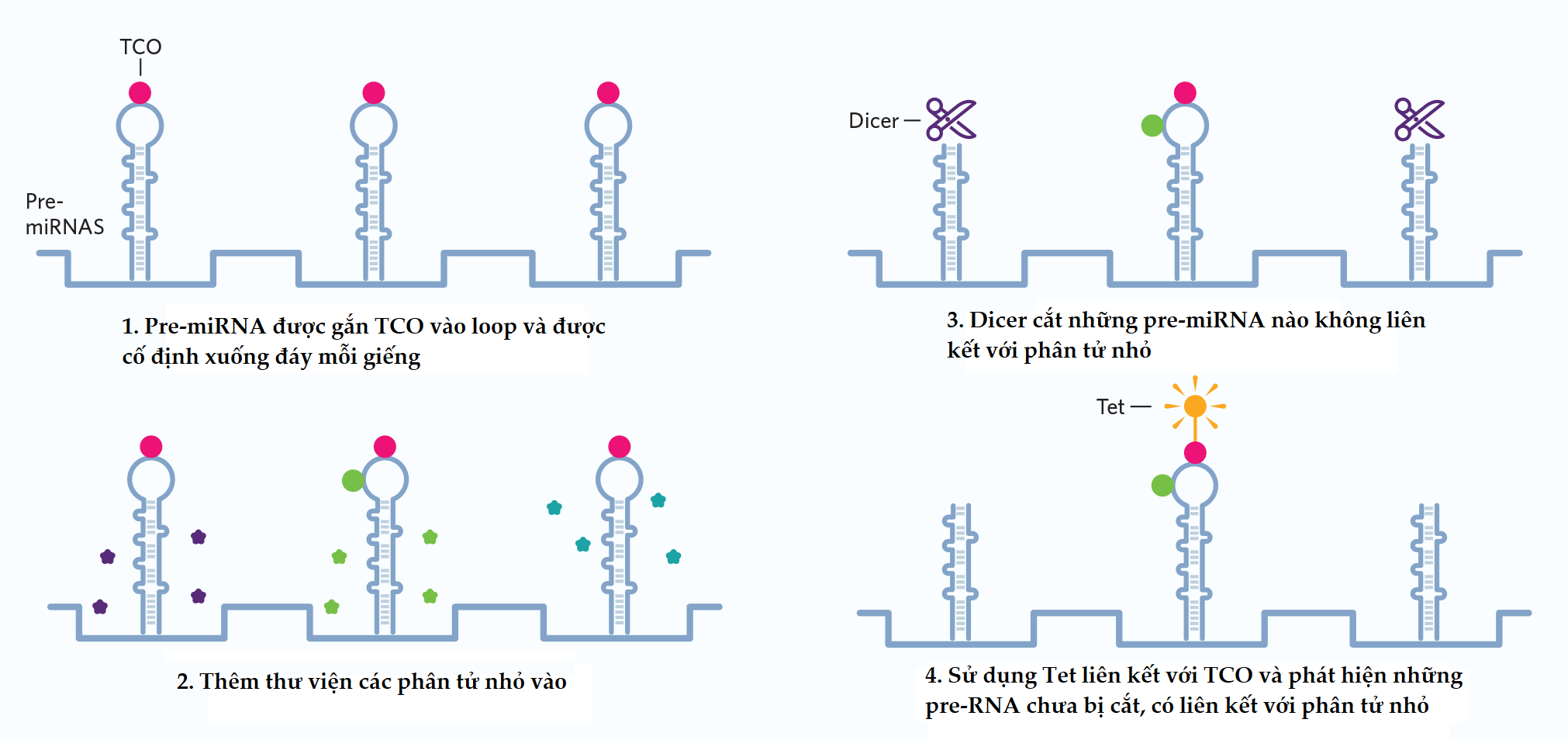
Bước đầu tiên là liên kết những pre-miRNA quan tâm với chỉ thị phân tử để nó có thể được phát hiện sau đó. Ở vòng loop của cấu trúc kẹp tóc, Garner đính vòng 8-carbon gọi là TCO (trans-cyclooctene). Cô cố định pre-miRNA đã được đánh dấu này vào đáy của 384 giếng. Sau đó, Garner thêm các chất khác nhau từ danh mục các hóa chất tiềm năng, để chúng có cơ hội gắn với miRNA. Sau đó, cô thêm Dicer, enzyme chịu trách nhiệm cắt pre-miRNA để hoạt hóa chúng thành dạng hoạt động.
Dicer cắt bất kỳ cấu trúc kẹp tóc nào chúng gặp, làm rơi vùng loop chứa TCO ra (màu hồng). Những miRNA liên kết được với phân tử nhỏ (màu xánh lá), tuy nhiên, lại được bảo vệ khỏi lưỡi hái Dicer. Cuối cùng, Garner thêm peroxydase của cây cải ngựa (horsreadish) liên kết với tetrazine (màu vàng), phức hợp này có thể liên kết được với TCO. Hoạt tính của peroxidase chỉ có ở những giếng chứa miRNA chưa bị cắt loop, chúng được nhận biết nhờ thử nghiệm quang hóa (chemiluminescent assay), khi đó các giếng phát sáng được xác định nhờ thiết bị đọc đĩa-384 giếng. Bất kỳ giếng nào phát sáng đều là những ‘cú hit’ tiềm năng (Hình 2).
Trong một nghiên cứu gần đây, Garner sử dụng cat-ELCCA để sàng lọc các hợp chất ngăn chặn sự phân cắt pre-miRNA cho miR-21, microRNA này biểu hiện quá mức trong đa phần các loại ung thư. Trong khoảng 83.000 phân tử nhỏ và các sản phẩm tự nhiên, bà báo cáo 1.819 chất tiềm năng, trong đó 217 chất được xác nhận sau ba lần thử nghiệm.
Thế nhưng gắn vào một RNA cụ thể thôi chưa đủ, nó còn phải có tính đặc hiệu, nghĩa là không ảnh hưởng tới những RNA khác. Để đạt được độ đặc hiệu, Garner và đồng nghiệp đã kiểm tra các phân tử gắn với miR-21 có sự tương tác với một pre-miRNA đối chứng, gọi là pre-let7-d hay không. Một vài dịch chiết tự nhiên có tính chọn lọc đối với miR-21, và Garner làm việc cùng các cộng tác viên để xác định chất nào mới thực sự là chất có tiềm năng trở thành thuốc chữa ung thư đích thực. (SLAS Discov, 23:47–54, 2018).
Thuốc thiết kế
Không phải ai cũng có thể truy cập đến một thư viện hóa học lớn. Và hầu hết những thư viện phân tử nhỏ được thiết kế cho mục tiêu protein dựa trên hiểu biết riêng cá nhân mỗi người, theo nhà sinh hóa Matt Disney thuộc Viện Scripps Research Institute ở Jupiter, Florida, và là đồng sáng lập công ty Expansion Therapeutics – một công ty chuyên phát triển thuốc trúng đích những RNA mang trình tự lặp lại nhiều lần liên tục gây bệnh (pathologically expanded RNA repeats). Điều đó, làm thông số phù hợp nhất cho protein mục tiêu có lẽ đã không được áp dụng đến cho RNA. Ví dụ, phân tử gắn với RNA có thể không yêu cầu chung một tiêu chuẩn khắt khe về mặt trọng lượng phân tử – thường ít hơn 500 daltons – thiết lập cho thuốc trúng đích protein.
Disney dùng phương pháp thiết kế hợp lý (rational design approach) cho những RNA mục tiêu. Phòng thí nghiệm anh đã thiết kế một quy trình để xác định và khám phá sự tương tác hứa hẹn giữa RNA và các phân tử nhỏ. (J Am Chem Soc, doi: 10.1021/jacs.8b13419, 2019).
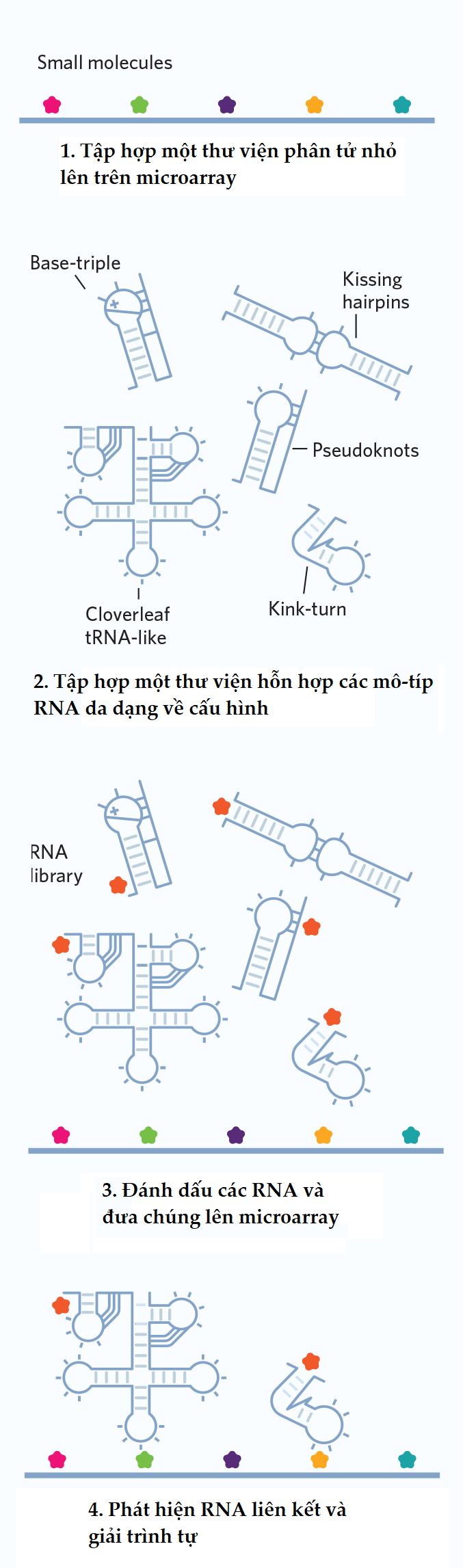
Bắt đầu với sàng lọc kết hợp hai chiều (2-dimensional combinatorial screening), viết tắt là 2DCS (J Am Chem Soc, 130:11185–94, 2008). Ý tưởng của Disney là phân thành hai thư viện – một cho cấu trúc đa dạng của các RNA và một cho các phân tử nhỏ – dựa vào sự tương tác lẫn nhau bằng cách cố định phân tử nhỏ lên microarray, và phơi nhiễm chúng với một hỗn hợp gồm hàng chục ngàn mô típ RNA. Những RNA này được gắn huỳnh quang hoặc thành phần phóng xạ, như vậy mỗi ‘cú hit’ được xem như là sự liên kết thành công giữa phân tử nhỏ và mô típ RNA, tạo ra những đốm sáng có thể thấy trên microarray. Các nhà nghiên cứu sau đó sẽ cắt những đốm sáng này ra và sử dụng giải trình tự RNA để xác định chúng (Hình 3).
Tiếp theo đến xử lý dữ liệu. Nhóm Disney phát triển một lịch trình thống kê gọi là HiT-StARTS, viết tắt của High Throughput Structure–Activity Relationships Through Sequencing. Về cơ bản, HiT-StARTS xử lý tập dữ liệu bằng cách ấn định điểm ái lực tương đối cho mỗi cặp mô típ RNA-phân tử nhỏ (ACS Cent Sci, 3:205–16, 2017).
Sau đó họ đăng tải dữ liệu và trình tự RNA lên cơ sở dữ liệu Inforna, có thể truy cập cơ sở này qua website của Disney (Nat Chem Biol, 10:291–97, 2014). Cở sở dữ liệu này hiện gồm khoảng 40,000 tương tác RNA-phân tử nhỏ, và thường xuyên được cập nhật thêm. Inforna là cơ sở dữ liệu nơi để chọn ra tương tác RNA-phân tử nhỏ tốt nhất.
Inforna đã chỉ ra vài RNA là mục tiêu cho thuốc tiềm năng. Các nhà nghiên cứu có thể cũng tiếp cận Inforna với một RNA cụ thể được biết tới dựa trên hiểu biết cá nhân, và tìm kiếm phân tử nhỏ và những khe/rãnh liên kết có thể có để thử.
Ví dụ, nhóm Scripps đã dùng Inforna để xác định các hợp chất gốc tiềm năng (lead compound) cho chứng loạn dưỡng tăng trương lực cơ (myotonic dystrophy – là một trong những bệnh thuộc hội chứng loạn dưỡng cơ muscular dystrophies), một căn bệnh hủy hoại cơ khởi phát ở người trưởng thành được mô tả với tình trạng cơ căng cứng không thể giãn ra. Nguyên nhân của bệnh là do sự lặp lại bất thường ba nucleotide CTG trong gen DMPK, dẫn đến mRNA chứa hàng trăm hoặc hàng ngàn các nucleotide CUG lặp lại liên tiếp. RNA mang các CUG lặp lại này dính chặt với một nhân tố cắt nối (splicing factor), can thiệp vào quá trình xử lý ở các mRNA khác.
Những RNA lặp lại bất thường này tự gấp cuộn lại với chính nó, hình thành cấu trúc thứ cấp nhờ một loạt các nucleotide C≡G tự bắt cặp bổ sung với nhau, trong khi U không liên kết thì nhô ra ngoài. Nhóm của Disney sử dụng Inforna để thiết kế phân tử nhỏ gắn lên chuỗi mRNA bất thường này, nhưng không gắn được với sợi phiên mã DMPK bình thường. Sau đó, đi đến một phân tử trong thư viện các phân tử nhỏ, chúng đính vào kháng sinh có hoạt tính chống u gọi là bleomycin – thuốc này có thể phân cắt acid nucleic do tạo ra các gốc superoxide và hydroxyl. Khi kết hợp với một phân tử nhỏ khác, gọi là cugamycin, phức chất này tìm và cắt các RNA bất thường gây bệnh (Nat Chem Biol, 13:188–93, 2017). Khi tiêm vào mô hình chuột loạn dưỡng tăng trương lực cơ, cugamycin đã điều chỉnh sự kiện lắp ghép-mRNA-sai gây nên bệnh (disease-linked RNA mis-splicing events) về lại trạng thái bình thường và làm thuyên giảm chứng căng cứng cơ (PNAS, 116:7799–804, 2019).
Thử nghiệm in vitro
Một hợp chất gốc (lead compound) liên kết với RNA trong ống nghiệm có thể không có hoạt tính giống như khi nó đi vào tế bào, vì vậy rất cần phải xác nhận lại hoạt tính phân tử nhỏ trong hệ thống sống, và kiểm tra xem liệu nó có gắn trật mục tiêu khác hay không. Disney cũng có một bộ công cụ sơ khởi trả lời cho câu hỏi này.
Một phương án làm lắng đọng nhờ vào kỹ thuật chemical cross-linking and isolation, viết tắt là Chem-CLIP (Angew Chem Int Ed Engl, 52:1001–13, 2013). Các nhà nghiên cứu móc nối phân tử nhỏ liên kết với RNA bằng một tác nhân tạo liên kết chéo (liên phân tử) như tác nhân alkyl hóa chlorambucil, và một tác nhân khác thuận tiện cho việc làm lắng xuống (tủa) là biotin. Tác nhân liên kết chéo làm cho phân tử nhỏ bám vào trình tự RNA mục tiêu bằng liên kết cộng hóa trị. Các nhà khoa học sau đó có thể làm lắng đọng RNA đã liên kết xuống, phân lập và xác định chúng bằng giải trình tự.
Đối với các nhà nghiên cứu không muốn mày mò với mớ hóa chất có trong kỹ thuật Chem-CLIP, Disney phát triển một phương án khác, gọi là lập bản đồ vị trí liên kết phối tử oligonucleotide đối mã (antisense oligonucleotide ligand binding site mapping), viết tắt là ASO-Bind-Map, để kiểm tra sự tương tác giữa phân tử nhỏ với những RNA chuyên biệt (Chem, 4:2384–404, 2018). Nguyên tắc là xem phân tử nhỏ muốn chấn vấn có gắn với trình tự mục tiêu và ngăn chặn sự liên kết của sợi oligonucleotide đối mã (antisense oligonucleotide – ASO). Nếu ASO không thể gắn, nó không thể xúc tác sự phân hủy RNA mà phù hợp với trình tự của nó. Trong ASO-Bind-Map, các nhà nghiên cứu xử lý các tế bào với phân tử nhỏ và hàng loạt ASO cho RNA mục tiêu. Sau đó họ có thể khuếch đại và giải trình tự RNA mục tiêu đó, tìm kiếm những vùng trên RNA mà được bảo vệ khỏi sự phân hủy qua trung gian ASO.
Ngay cả với những tiến bộ này gần đây, bộ công cụ phát triển thuốc tác động RNA còn rất xa mới có thể hoàn thiện. Disney cho rằng ngành công nghiệp dược phẩm sẽ cần nhiều thử nghiệm hơn vậy để xác nhận mục tiêu. Và Week hy vọng cải thiện khả năng của kỹ thuật SHAPE để phỏng đoán cấu trúc bậc ba của RNA. Công cụ của Week và Disney có thể cùng phối hợp để sàng lọc, Garner viết, nếu các nhà khoa học sử dụng chúng để xác định những vùng tiềm năng trên RNA – các khe/rãnh rất có thể là nơi gắn thuốc – sau đó họ sử dụng vùng đó như là mồi trong sàng lọc của họ.
Các chương trình như thuốc teo cơ tủy—hiện nay đang trong giai đoạn thử nghiệm lâm sàng—và các chất tiềm năng khác được xác định bởi các nhà khoa học cho thấy nó là sự bổ sung đáng giá cho bộ công cụ. “Tất cả những thứ này nói lên rằng, ừ, “Bạn có thể sử dụng RNA với các phân tử nhỏ,” Disney nói. “Và chúng ta thực sự cần phải làm điều đó.”
Cao Hồng Chiến (chuyển ngữ)
Phạm Trường Duy, Duy Trần, Joseph Ngo (hiệu đính)
Bài báo:
Amber Dance. Drug Discovery Techniques Open the Door to RNA-targeted Drugs. The Scientist. Jun 1, 2019.